蛋白质的双缩脲反应(实验原理简单、比较容易操作。)是一个反应原理较为简单,较为容易进行的实验。这里介绍一下这个反应的原理,实验过程十分安全,大家有实验条件的可以自行在家中尝试。
首先,当尿素加热到180℃时,2分子尿素缩合,放出1分子氨,形成双缩脲。反应方程如图所示: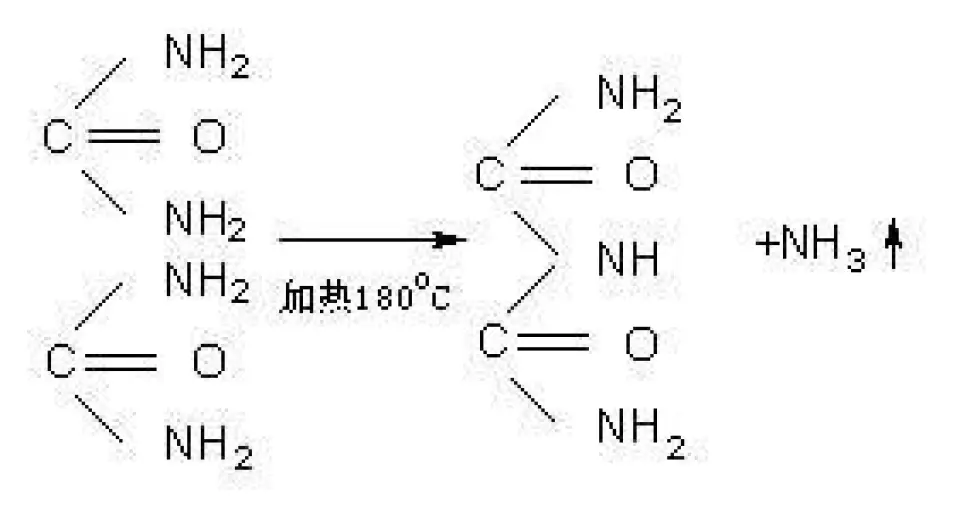
双缩脲中含有-CO-NH-,在碱性条件下可以与Cu2+螯合形成螯合物,该螯合物为紫红色。其结构如图所示:
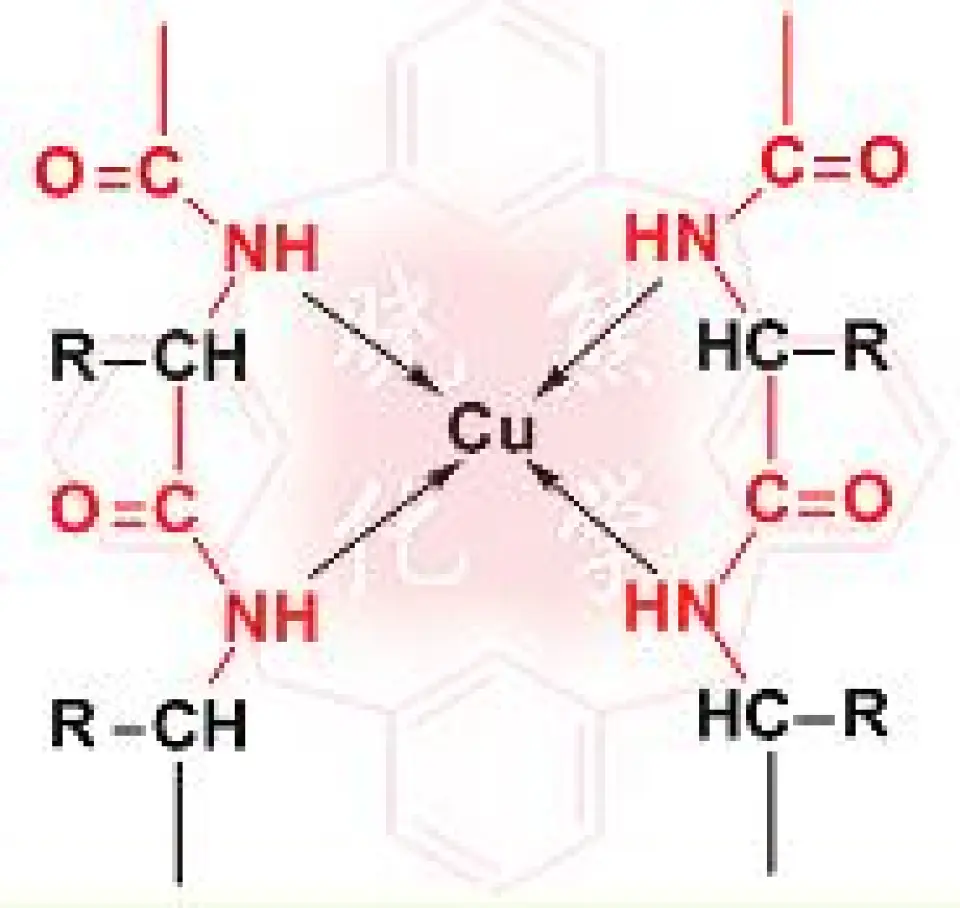
看到这里,大家应该能意识到该实验检测蛋白质的依据是什么了。因为蛋白质是由多个氨基酸以肽键链接而成的,所以二肽以上的多肽分子中含有多个与双缩脲结构相似的结构。固蛋白质或二肽以上的多肽也可以在碱性条件下与Cu2+反应生成紫红色物质,且颜色深浅与蛋白质含量成正相关。但是这同时说明,具有相似结构的物质都会影响到实验的结果,如含有-CS-NH2、-CH2-NH2、-CRH-NH2等基团的物质或含有过量铵盐的物质都会对此反应产生干扰。
从上述实验原理我们可以看出,氨基酸并不能进行此反应,所以该反应也可以用来检测蛋白质的水解程度。
详细的实验步骤如下:
① 取1支试管,加入少许尿素,试管口放一片湿润的石蕊试纸,加热至试纸变为蓝色,且试管内物质蒸干后停止加热。冷却后用吸量管加入10%的NaOH试剂1ml摇匀,再加入2~4滴1%的CuSO4,摇匀观察溶液颜色变化。
② 取1支试管,加入稀释后的鸡蛋清。用吸量管加入10%的NaOH试剂1ml摇匀,再加入2~4滴1%的CuSO4,摇匀观察溶液颜色变化。(需要准备:药匙、吸量管、洗耳球、试管夹、试管架、尿素、NaOH、CuSO4)
PS:自己在家中进行实验的话,可以用鸡蛋清的稀释液进行蛋白质的检测。在实验过程中需要注意的是,配制双缩脲试剂时,应避免CuSO4过量生成蓝色的Cu(OH)2,其颜色会对结果产生干扰。有条件的可以尝试用氨基酸和双缩脲进行反应。
作者:神州
审核:未名